2
|
ΠΕΡΙΕΧΟΜΕΝΑ 2.1 Μεταβολή ενέργειας κατά τις χημικές αντιδράσεις -Ενδόθερμες, εξώθερμες αντιδράσεις - Θερμότητα αντίδρασης - Ενθαλπία 2.2 Θερμιδομετρία - Νόμοι θερμοχημείας Ερωτήσεις - προβλήματα |
 |
2
ΕΝΕΡΓΕΙΑΚΕΣ ΜΕΤΑΒΟΛΕΣ
|
2.1 Μεταβολή ενέργειας κατά τις χημικές μεταβολές
Κάθε ουσία, εκτός από άτομα μόρια ή ιόντα, «κουβαλά» ενέργεια, τη χημική ενέργεια. Η χημική ενέργεια οφείλεται στις δυνάμεις του δεσμού (που συγκρατούν τα άτομα στο μόριο), στις έλξεις των μορίων και των υποατομικών σωματιδίων, στην κίνηση των ατόμων, μορίων και ηλεκτρονίων κλπ. Είναι, δηλαδή, συνδυασμός κινητικής και δυναμικής ενέργειας. Η χημική ενέργεια είναι μια «κρυμμένη» μορφή ενέργειας και μέρος αυτής μπορεί να αποδοθεί άλλοτε εύκολα (π.χ. στη βενζίνη με ένα σπινθήρα) και άλλοτε δύσκολα (π.χ. στα πυρηνικά καύσιμα) στο περιβάλλον. |
 Σύστημα είναι ο χώρος που γίνεται η αντίδραση. Οτιδήποτε άλλο εκτός αυτού ονομάζεται περιβάλλον. • Θερμότητα είναι η ενέργεια που μεταφέρεται από ένα σύστημα σ’ ένα άλλο λόγω διαφοράς θερμοκρασίας. Η θερμότητα μετριέται σε μονάδες ενέργειας, όπως είναι : • Θερμοκρασία είναι το μέτρο κίνησης των δομικών μονάδων της ύλης π.χ. των μορίων. |
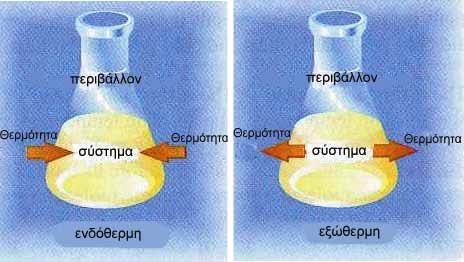 Οι εξώθερμες αντιδράσεις ελευθερώνουν θερμότητα, ενώ οι ενδόθερμες απορροφούν. Η καύση των υδρογονανθράκων αποτελεί χαρακτηριστικό παράδειγμα εξώθερμης αντίδρασης. Έτσι, κατά την καύση 1 mol μεθανίου (CH4)., ελευθερώνεται ποσό θερμότητας ίσο με 890 kJ. Η αντίδραση αυτή μπορεί να εκφραστεί με την παρακάτω θερμοχημική εξίσωση: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) + 890 kJ
Κατά την καύση του μεθανίου ελευθερώνεται ενέργεια υπό μορφή θερμότητας, επειδή τα αντιδρώντα έχουν μεγαλύτερο ενεργειακό περιεχόμενο από τα προϊόντα, όπως φαίνεται στο παρακάτω σχήμα: 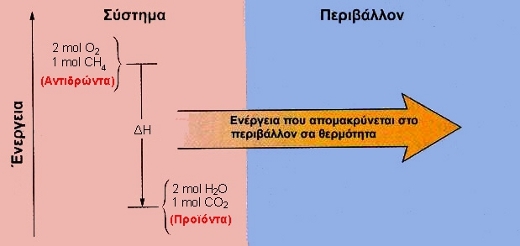 ΣΧΗΜΑ 2.2 Η καύση του μεθανίου είναι εξώθερμη αντίδραση.
Το ποσό της θερμότητας που ελευθερώνεται είναι η διαφορά του ενεργειακού περιεχομένου μεταξύ των αντιδρώντων (1 mol CH4(g) και 2 mol O2(g)) και των προϊόντων (1 mol CO2(g) και 2 mol H2O(l)). Για να ξεκινήσει βέβαια η καύση απαιτείται ένα ελάχιστο ποσό ενέργειας, για το οποίο όμως θα γίνει λόγος στο επόμενο κεφάλαιο. |
Αυτό που μας ενδιαφέρει και μετράμε κατά τις χημικές αντιδράσεις, είναι η μεταβολή της ενέργειας και όχι οι ενέργειες αντιδρώντων και προϊόντων. Αυτή η μεταβολή ενέργειας κατά τη χημική αντίδραση είναι γνωστή ως μεταβολή της ενθαλπίας και συμβολίζεται με ΔΗ. Η μεταβολή της ενθαλπίας ΔΗ ισούται με το απορροφούμενο ή εκλυόμενο ποσό θερμότητας q, εφόσον η αντίδραση πραγματοποιείται υπό σταθερή πίεση.
Σε μια ενδόθερμη αντίδραση:
Η μεταβολή της ενθαλπίας ΔΗ = Ητελ – Ηαρχ > 0 γιατί Ητελ > Ηαρχ Σε μια εξώθερμη αντίδραση: Η μεταβολή της ενθαλπίας ΔΗ = Ητελ – Ηαρχ < 0 γιατί Ηαρχ > Ητελ
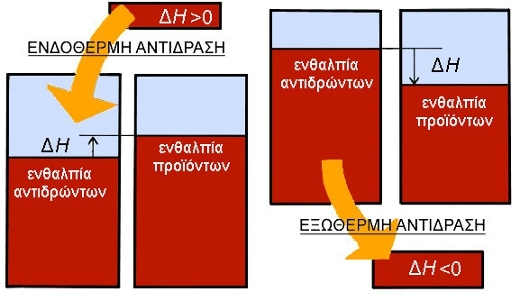 ΣΧΗΜΑ 2.3 Η ενθαλπία είναι σαν ένα «ντεπόζιτο» που περιέχει την ενέργεια του αντιδρώντος συστήματος. Το «ντεπόζιτο» αυτό γεμίζει στις ενδόθερμες αντιδράσεις και αδειάζει στις εξώθερμες.
Ενθαλπία αντίδρασης - ΔΗ Για μια αντίδραση της γενικής μορφής αΑ + βΒ → γΓ + δΔ, |
Ενθαλπία - Η 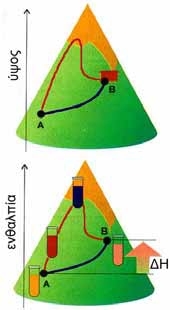 Το γεωγραφικό ύψος, όπως και η ενθαλπία, είναι καταστατικές ιδιότητες. Η τιμή που τελικά παίρνουν σε μια θέση δε «κοιτάζει» τη διαδρομή που ακολουθεί το σύστημα για να φτάσει στη θέση αυτή. • Να προσέξουμε ότι η ενθαλπία δεν είναι θερμότητα. Ένα σώμα έχει ενθαλπία, αλλά όχι θερμότητα. Θερμότητα δίνει ή παίρνει ένα σώμα με αποτέλεσμα να αλλάζει η ενθαλπία του. |
Η μεταβολή της ενθαλπίας μιας αντίδρασης εξαρτάται: Ενθαλπία αντίδρασης ορίζεται η μεταβολή ενθαλπίας ΔΗ μεταξύ των αντιδρώντων και προϊόντων, για δεδομένες συνθήκες πίεσης και θερμοκρασίας.
Δηλαδή, ΔΗ = Η προϊόντων - Η αντιδρώντων Η ενθαλπία μιας αντίδρασης αναφέρεται στην αντίδραση, όπως αυτή αναγράφεται στη χημική εξίσωση.
Πρότυπη ενθαλπία αντίδρασης, ΔΗ ο Η μεταβολή της ενθαλπίας σε μια χημική αντίδραση, προφανώς εξαρτάται από τις συνθήκες που βρίσκονται τόσο τα αντιδρώντα όσο και τα προϊόντα. Για συγκριτικούς λοιπόν λόγους θα πρέπει οι μεταβολές ενθαλπίας να ανάγονται στις ίδιες συνθήκες. Με διεθνή σύμβαση έχει καθοριστεί οι μεταβολές αυτές να αναφέρονται σε αντιδρώντα και σε προϊόντα που βρίσκονται στην πρότυπη τους κατάσταση.
|
• Γενικά μεταβολή μεγέθους ΔΧ ορίζεται: |
Η πρότυπη κατάσταση μιας ουσίας (στοιχείου ή ένωσης) είναι η πιο σταθερή μορφή της σε
Παρακάτω ορίζονται οι μεταβολές της ενθαλπίας για ορισμένες χαρακτηριστικές περιπτώσεις. Πρότυπη ενθαλπία σχηματισμού, ΔΗ of
Η ΔΗ of των στοιχείων στην πιο σταθερή μορφή τους θεωρείται μηδέν π.χ. ΔΗ of(γραφίτης) = 0, ενώ ΔΗ of(διαμαντιού) ≠ 0. Επίσης η τιμή της ΔΗ o μιας αντίδρασης μπορεί να υπολογιστεί με βάση τις πρότυπες ενθαλπίες σχηματισμού των ενώσεων που μετέχουν στην αντίδραση: ΔΗ o = ΣΔΗ of(προϊόντων) - ΣΔΗ of (αντιδρώντων)
Π.χ. για την αντίδραση 2ΝΗ3(g) +3Cl2(g) →N2(g) +6HCl(g) ισχύει 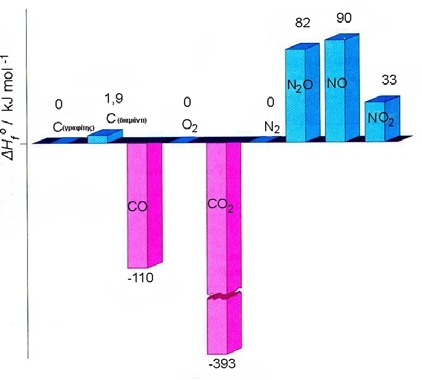 |
|
Πρότυπη ενθαλπία καύσης, ΔΗοc
Π.χ. όταν λέμε ότι η ενθαλπία καύσης του C3H8 είναι -2220 kJ mol-1, εννοούμε ότι: Παράδειγμα 2.1 Κατά την πλήρη καύση 4 g CH4 ελευθερώνεται θερμότητα 222,5 kJ. Ποια είναι η τιμή της ΔΗοc της αντίδρασης; ΛΥΣΗ Εφαρμογή Καίγονται 22g προπανίου οπότε ελευθερώνονται 110 kcal. Ποια είναι η τιμή της ΔΗοc της καύσης του προπανίου; Πρότυπη ενθαλπία εξουδετέρωσης, ΔΗοn
Να σημειωθεί ότι η ΔΗοn παίρνει πάντα αρνητική τιμές. Άρα, η αντίδραση εξουδετέρωσης είναι εξώθερμη αντίδραση. Επίσης κατά την εξουδετέρωση ισχυρού οξέος με ισχυρή βάση η τιμή της ΔΗοn είναι περίπου σταθερή, ανεξάρτητα από το είδος του οξέος ή της βάσης που χρησιμοποιούμε. Δηλαδή, |
Αυτό συμβαίνει γιατί τα ισχυρά οξέα και οι ισχυρές βάσεις διίστανται (ή ιοντίζονται) πλήρως σε ιόντα και η μόνη αντίδραση που γίνεται κατά την εξουδετέρωση είναι: Παράδειγμα 2.2 Πόση θερμότητα ελευθερώνεται αν εξουδετερωθούν 10 L διαλύματος HCl 0,01 M από διάλυμα NaOH 0,02 Μ και ποιος ο τελικός όγκος του διαλύματος; Δίνεται ότι η θερμότητα εξουδετέρωσης του HCl με NaOH είναι ίση με: ΔΗοn = -57,1 kJ mol-1. ΛΥΣΗ Εφαρμογή Πόσα λίτρα διαλύματος ΗΝΟ3 0,04 Μ χρειάζονται για να εξουδετερώσουν πλήρως 5 L διαλύματος NaOH 0,01 M και πόση θερμότητα θα ελευθερωθεί; Δίνεται ότι η θερμότητα εξουδετέρωσης του HNO3 με NaOH είναι ίση με ΔΗοn = -57,1 kJ. |
• Θυμηθείτε από την ύλη της Α΄ λυκείου τη θεωρία ηλεκτρολυτικής διάστασης του Arrhenius |
Πρότυπη ενθαλπία διάλυσης, ΔΗοsol
π.χ. NaCl(s) → Na+(aq) + Cl-(aq) ΔΗοsol = + 4 kJ Γενικότερα, η διάλυση μιας ουσίας σε ένα διαλύτη περιλαμβάνει τα εξής βήματα, όπως διαγραμματικά απεικονίζεται στην περίπτωση μιας ετεροπολικής (ιοντικής) ένωσης: 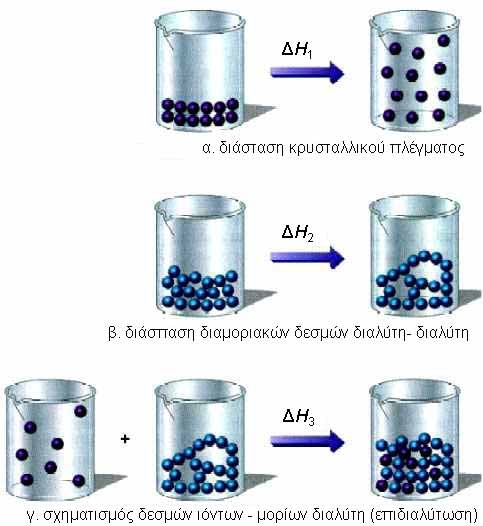 |
• Αν διαλύσουμε 1 mol ουσίας σε 1 L διαλύτη θα παρατηρηθεί διαφορετική τιμή ΔΗ από αυτή που προκύπτει κατά τη διάλυση 1 mol ουσίας σε 2 L διαλύτη. Γι’ αυτό και ο ορισμός της ΔΗοsol βασίζεται στη διάλυση της ουσίας σε μεγάλη περίσσεια διαλύτη, ώστε η παραπέρα προσθήκη διαλυτικού μέσου να μην προκαλεί καμιά θερμική μεταβολή στο σύστημα. Εφυδάτωση ιόντων Na+ και Cl-. 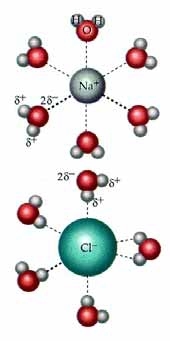 ΣΧΗΜΑ 2.5 |
Ενθαλπία δεσμού, ΔΗB Η ενθαλπία δεσμού αποτελεί το μέτρο της ισχύος ενός χημικού δεσμού.
π.χ. Cl - Cl (g) → 2Cl (g) ΔΗoB = +242 kJ Οπότε, ισχύει: ΔΗ αντίδρασης = ΣΔΗ δεσμών που διασπώνται - ΣΔΗ δεσμών που σχηματίζονται
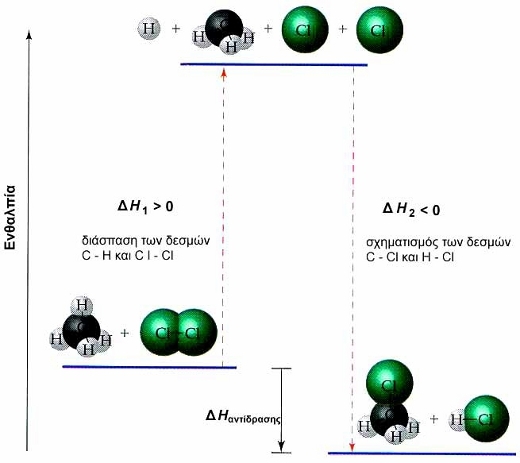 ΣΧΗΜΑ 2.6 Η ενθαλπία αντίδρασης CH4 + Cl2 → CH3Cl + HCl ισούται με ΔΗ = ΔΗ1+ΔΗ2 , όπου ΔΗ1 η ενέργεια που απαιτείται για τη διάσπαση των δεσμών C-H, Cl-Cl και ΔΗ2 η ενέργεια που ελευθερώνεται για το σχηματισμό των δεσμών C-Cl και H-Cl. |
Ενθαλπία δεσμών (ΔΗB σε kJ mol-1 ) στα μόρια των στοιχείων αζώτου, οξυγόνου και φθορίου. Παρατηρούμε ότι η ενθαλπία των δεσμών εξασθενίζει από τον τριπλό στον απλό δεσμό.
Ενθαλπία δεσμών (ΔΗB σε kJ mol-1 ) στα μόρια των υδραλογόνων υδροφθορίου, υδροχλωρίου, υδροβρωμίου και υδροϊωδίου. Παρατηρούμε ότι η ενθαλπία δεσμού ελαττώνεται όσο αυξάνεται το μέγεθος του ατόμου του αλογόνου (ατομική ακτίνα) |