Η Βιοτεχνολογία με αριθμούς
Η ετήσια αγορά των ανασυνδυασμένων φαρμακευτικών προϊόντων έφτανε στα τέλη του 1997 τα 150.000.000.000 δολάρια.
Εφαρμογές της Βιοτεχνολογίας
|
κεφάλαιο 8
8. Εφαρμογές της Βιοτεχνολογίας Η Βιοτεχνολογία έχει συμβάλλει αποτελεσματικά σε τρεις βασικούς στόχους της Ιατρικής, που είναι η έγκαιρη διάγνωση μιας ασθένειας, η πρόληψη και η αποτελεσματική θεραπεία της. Η έγκαιρη διάγνωση μιας ασθένειας απαιτεί την ανάπτυξη ευαίσθητων τεχνικών που μπορούν να εντοπίσουν την ασθένεια στα αρχικά της στάδια, πριν να εμφανιστούν τα συμπτώματά της στον οργανισμό, να ανιχνεύσουν κάποια μόλυνση από παθογόνους οργανισμούς ή να διαπιστώσουν την ύπαρξη κάποιας κληρονομικής ασθένειας. Η πρόληψη σοβαρών ασθενειών όπως η ηπατίτιδα Β, η πολιομυελίτιδα και η φυματίωση χρειάζεται πιο εξελισμένα, επαρκώς ασφαλή αλλά και οικονομικά προσιτά εμβόλια. Επίσης η ανάπτυξη εμβολίων για την πρόληψη ασθενειών όπως το AIDS, η μηνιγγίτιδα και ο καρκίνος είναι πλέον επιτακτική ανάγκη. Η αποτελεσματική θεραπεία προϋποθέτει την κατανόηση των βιοχημικών μηχανισμών και του γενετικού υπόβαθρου της ασθένειας, για να εφαρμοστεί η κατάλληλη θεραπεία είτε με φαρμακευτική αγωγή είτε ακόμη και με «γενετική διόρθωση» της βλάβης. Η Βιοτεχνολογία συνεισφέρει ουσιαστικά στους παραπάνω στόχους με την ανάπτυξη της τεχνολογίας του ανασυνδυασμένου DNA, με τη χρήση της τεχνικής PCR, καθώς και ανιχνευτών μορίων DNA. Οι τεχνικές αυτές βρίσκουν εφαρμογή στη βελτίωση και παραγωγή σε ευρεία κλίμακα ευαίσθητων διαγνωστικών ουσιών όπως τα μονοκλωνικά αντισώματα, αποτελεσματικών εμβολίων και φαρμακευτικών προϊόντων. Πρόσφατα, ένας νέος τομέας της Βιοτεχνολογίας αναπτύσσεται ταχύτατα, η γονιδιακή θεραπεία, που στηρίζεται στην εφαρμογή της τεχνολογίας του ανασυνδυασμένου DNA στη θεραπεία πολλών σοβαρών γενετικών ασθενειών όπως η κυστική ίνωση, το σύνδρομο επίκτητης ανοσολογικής ανεπάρκειας (AIDS) και διάφοροι τύποι καρκίνου. Πλήθος «φαρμακευτικών» πρωτεϊνών συντίθενται από βακτήρια με μεθόδους Γενετικής ΜηχανικήςΠριν από την ανάπτυξη της τεχνολογίας του ανασυνδυασμένου DNA, οι περισσότερες φαρμακευτικές πρωτεΐνες, δηλαδή πρωτεΐνες που χρησιμοποιούνται για τη θεραπεία διάφορων ασθενειών, ήταν διαθέσιμες σε πολύ μικρές ποσότητες, η παραγωγή τους ήταν πολύ ακριβή και συχνά η βιολογική δράση τους δεν ήταν πλήρως κατανοητή. Η τεχνολογία του ανασυνδυασμένου DNA έδωσε τη δυνατότητα παραγωγής φαρμακευτικών πρωτεϊνών σε σημαντικές ποσότητες, τόσο για τον αποτελεσματικό έλεγχο της δράσης τους όσο και για ευρεία κατανάλωση. Η Βιοτεχνολογία με αριθμούςΗ ετήσια αγορά των ανασυνδυασμένων φαρμακευτικών προϊόντων έφτανε στα τέλη του 1997 τα 150.000.000.000 δολάρια.
Σήμερα έχουν κλωνοποιηθεί τα γονίδια του ανθρώπου για περισσότερες από 300 φαρμακευτικές πρωτεΐνες. Στον πίνακα 8.1 αναγράφονται ορισμένες φαρμακευτικές πρωτεΐνες που έχουν παραχθεί με την τεχνολογία του ανασυνδυασμένου DNA και η χρήση τους. Μεταξύ των πρώτων μορίων που παρασκευάστηκαν είναι η ινσουλίνη, οι ιντερφερόνες και η αυξητική ορμόνη. Η ινσουλίνη είναι μια ορμόνη που αποτελείται από 51 αμινοξέα και παράγεται από ειδικά κύτταρα του παγκρέατος. Η ορμόνη αυτή ρυθμίζει το μεταβολισμό των υδατανθράκων και ειδικότερα το ποσοστό της γλυκόζης στο αίμα. Ο διαβήτης είναι μια ασθένεια που χαρακτηρίζεται από έλλειψη ή μείωση ινσουλίνης και υπολογίζεται ότι πάνω από 60.000.000 άτομα στον κόσμο πάσχουν από διαβήτη. |
||||||||||||||||||||||||||||||||
Η ινσουλίνη χρησιμοποιείται για τη θεραπεία των διαβητικών ατόμων. Πριν από το 1982 οι κύριες πηγές ινσουλίνης ήταν το πάγκρεας από χοίρους και από βοοειδή. Η ινσουλίνη παραγόταν από την εκχύλιση αυτών των ιστών με μια δαπανηρή και πολύπλοκη διαδικασία και επιπλέον, επειδή είχε μικρές διαφορές στη σύσταση των αμινοξέων της από την ανθρώπινη, προκαλούσε αλλεργικές αντιδράσεις. Η ινσουλίνη αποτελείται από δύο μικρά πεπτίδια, Α και Β, που συγκρατούνται μεταξύ τους με δισουλφιδικούς δεσμούς. Το γονίδιο της ινσουλίνης παράγει ένα πρόδρομο μόριο, την προϊνσουλίνη, το οποίο μετατρέπεται τελικά σε ινσουλίνη. Μια από τις μεθόδους που χρησιμοποιούνται για την παραγωγή της ανθρώπινης ινσουλίνης στα βακτήρια είναι η παραγωγή του πρόδρομου μορίου της σε μια βακτηριακή καλλιέργεια και η μετατροπή της σε ινσουλίνη με ενζυμική κατεργασία (Εικ. 8.1). Η μέθοδος περιλαμβάνει την κατασκευή cDNA βιβλιοθήκης από τα κύτταρα του παγκρέατος στα οποία εκφράζεται το γονίδιο της ινσουλίνης και την επιλογή του κλώνου που περιέχει το γονίδιο. Συνοπτικά τα στάδια κλωνοποίησης και απομόνωσης του γονιδίου της ινσουλίνης είναι:
Δύο άλλες σημαντικές πρωτεΐνες, η αυξητική ορμόνη και η ερυθροποιητίνη. Παράγονται με μεθόδους Γενετικής ΜηχανικήςΗ αυξητική ορμόνη παράγεται στην υπόφυση του ανθρώπου και παίζει σημαντικό ρόλο στη φυσιολογική ανάπτυξή του. Η απουσία της ορμόνης αυτής οδηγεί σε νανισμό. Επειδή η ανθρώπινη αυξητική ορμόνη είναι πολύ ειδική και δεν μπορεί να αντικατασταθεί από την αντίστοιχη ορμόνη άλλων οργανισμών, απομονωνόταν από εγκεφάλους νεκρών ανθρώπων. Μετά το 1985 η αυξητική ορμόνη παράγεται με τις τεχνικές του ανασυνδυασμένου DNA όπως η ινσουλίνη και οι ιντερφερόνες. Πιστεύεται ότι η αυξητική ορμόνη θα έχει ευρεία εφαρμογή για τη θεραπεία τραυμάτων, σπασμένων οστών, καμένων ιστών και επίσης για την καθυστέρηση της απώλειας της μυϊκής μάζας, που συμβαίνει προοδευτικά κατά τη γήρανση του οργανισμού. Με τις ίδιες τεχνικές το 1989 παρασκευάστηκε η ερυθροποιητίνη, μια ορμόνη που παράγεται στους νεφρούς και μέσω της κυκλοφορίας του αίματος μεταφέρεται στο μυελό των οστών όπου επάγει την παραγωγή των κυττάρων του αίματος. Η ερυθροποιητίνη μπορεί να βοηθήσει στη θεραπεία ορισμένων αναιμιών. Εικόνα 8.1 Διαδικασία παραγωγής ινσουλίνης με μεθόδους Γενετικής Μηχανικής.
|
κεφάλαιο 8
Οι ιντερφερόνες είναι αντιιικές πρωτεΐνες, που παράγονται από κύτταρα που έχουν μολυνθεί από ιούς. Οι πρωτεΐνες αυτές, επάγουν την παραγωγή άλλων πρωτεϊνών από τα γειτονικά υγιή κύπαρα, οι οποίες εμποδίζουν τον πολλαπλασιασμό των ιών σ' αυτά. Οι ιντερφερόνες είναι οικογένεια συγγενών πρωτεϊνών, που ταξινομούνται ανάλογα με τη χημική και βιολογική ενεργότητα τους σε τρεις ομάδες: τις ιντερφερόνες, α, β και γ. Οι ιντερφερόνες έχουν ιδιαίτερο ενδιαφέρον ως αντιιικοί και πιθανόν ως αντικαρκινικοί παράγοντες. Παράγονται σε ελάχιστες ποσότητες στο σώμα και γΓ αυτό δεν ήταν ευρεία η χρήση τους στη θεραπεία ασθενειών. Όμως, μετά την κλωνοποίηση ορισμένων γονιδίων ιντερφερονών, είναι σήμερα δυνατή η παραγωγή τους σε μεγάλες ποσότητες, με παρόμοια μέθοδο παραγωγής με αυτή της ινσουλίνης. Μονοκλωνικά αντισώματα«Το ιδανικό φάρμακο», είπε ο πρωτοπόρος Γερμανός γιατρός Ehrlich, «πρέπει να μπορεί να εξουδετερώνει τις μολύνσεις χωρίς να προκαλεί παρενέργειες στον οργανισμό». Η φύση έχει φτιάξει ένα «τέλειο φάρμακο», τα αντισώματα. Τα αντισώματα είναι πρωτεϊνικά μόρια, που παράγονται από τα Β-λεμφοκύπαρα του ανοσοποιητικού μας συστήματος, όταν ένα αντιγόνο (παθογόνος μικροοργανισμός, ιός ή ξένο υλικό) προσβάλει τον οργανισμό. Τα αντισώματα αντιδρούν με το αντιγόνο και το εξουδετερώνουν. Ο οργανισμός μας είναι ικανός να παράγει αντισώματα εναντίον κάθε ξένου αντιγόνου. Στην πραγματικότητα, ένα αντίσωμα αναγνωρίζει μόνο μία περιοχή του αντιγόνου, η οποία ονομάζεται αντιγονικός καθοριστης. Ένα μεγάλο αντιγόνο, π.χ. ένας μικροοργανισμός, έχει πολλούς αντιγονικούς καθοριστές γι' αυτό παράγονται πολλά είδη αντισωμάτων εναντίον του. Κάθε είδος αντισώματος που αναγνωρίζει έναν αντιγονικό καθοριστή παράγεται από μια ομάδα όμοιων Β-λεμφοκυττάρων, που αποτελούν έναν κλώνο. Τα αντισώματα που παράγονται από έναν κλώνο Β-λεμφοκυπάρων ονομάζονται μονοκλωνικά. Τα μονοκλωνικά αντισώματα είναι πολύ σημαντικά στην Ιατρική και χρησιμοποιούνται ως διαγνωστικά για την ανίχνευση ασθενειών ή ως εξειδικευμένα φάρμακα εναντίον παθογόνων μικροοργανισμών ή ακόμη εναντίον καρκινικών κυττάρων. Ήταν, επομένως, σημαντικό να γίνει δυνατή η παραγωγή τους στο εργαστήριο σε μεγάλες ποσότητες. Όμως τα Β-λεμφοκύτταρα δεν επιβιώνουν για πολύ έξω από το σώμα και δεν μπορούν να διατηρηθούν σε κυτταροκαλλιέργειες. Την ιδιότητα αυτή την αποκτούν ύστερα από σύντηξη με καρκινικά κύτταρα. Τα υβριδικά κύτταρα που παράγονται ονομάζονται υβριδώματα και μπορούν να παράγουν μεγάλες ποσότητες ενός μονοκλωνικού αντισώματος. Η τεχνική της παραγωγής μονοκλωνικών αντισωμάτων αναπτύχθηκε το 1975 και ακολουθεί την εξής διαδικασία: Ένα επιλεγμένο αντιγόνο χορηγείται με ένεση σε ποντίκι και προκαλεί ανοσολογική αντίδραση με αποτέλεσμα να αρχίσει η παραγωγή αντισωμάτων από εξειδικευμένα Β-λεμφοκύτταρα. Ύστερα από δύο εβδομάδες αφαιρείται ο σπλήνας και απομονώνονται τα Β-λεμφοκύτταρα. Τα κύτταρα αυτά συντήκονται με καρκινικά κύτταρα και παράγονται τα υβριδώματα που παράγουν μονοκλωνικά αντισώματα. Τα υβριδώματα μπορούν να φυλάσσονται για μεγάλα χρονικά διαστήματα στην κατάψυξη (-80 °C) και να παράγουν οποιαδήποτε στιγμή το συγκεκριμένο μονοκλωνικά αντίσωμα σε μεγάλες ποσότητες (Εικόνα 8.2). Τα μονοκλωνικά αντισώματα έχουν πολυάριθμες εφαρμογές και λειτουργούν ως:
|
Εικόνα 8.2 Δημιουργία υβριδωμάτων για την παραγωγή μονοκλωνικών αντισωμάτων.
|
κεφάλαιο 8
Και άλλες εφαρμογές των αντισωμάτων Ανιχνευτές. Η εξέλιξη μιας ασθένειας ή η πρόοδος της θεραπείας της μπορεί να ελεγχθεί με τη βοήθεια των μονοκλωνικών αντισωμάτων. Ειδικοί επιστήμονες συνδέουν ραδιενεργά ισότοπα με αντισώματα, τα εισάγουν στον οργανισμό και ανιχνεύουν τη θέση των ραδιενεργών ισοτόπων στο σώμα. Η τεχνική αυτή μπορεί να χρησιμοποιηθεί για να προσδιοριστεί με ακρίβεια σε ποιο σημείο του σώματος υπάρχει ένας θρόμβος ή κάποιος όγκος. ΕμβόλιαΤα εμβόλια αποτελούνται από νεκρές ή από εξασθενημένες μορφές ενός παθογόνου μικροοργανισμού. Για το σκοπό αυτό, ο παθογόνος μικροοργανισμός αναπτύσσεται σε κυτταροκαλλιέργεια, απομονώνεται και είτε νεκρώνεται είτε απενεργοποιείται (γίνεται μη μολυσματικός), χωρίς βέβαια να χάνει την ικανότητά του να προκαλεί ενεργητική ανοσία. Μολονότι έχουν παραχθεί αποτελεσματικά εμβόλια για μια σειρά από ασθένειες όπως η διφθερίτιδα, ο τέτανος, η ευλογιά και η πολιομυελίτιδα, υπάρχουν πολλά μειονεκτήματα στην παραγωγή εμβολίων με τον παραπάνω τρόπο. Τα μειονεκτήματα αυτά είναι:
Την τελευταία δεκαετία η τεχνολογία του ανασυνδυασμένου DNA έδωσε τη δυνατότητα ανάπτυξης μιας νέας γενιάς εμβολίων που υπερνικούν τα μειονεκτήματα των παραδοσιακών. Η κλωνοποίηση των γονιδίων έδωσε τη δυνατότητα ανάπτυξης νέων στρατηγικών για την πρόκληση ισχυρής ενεργητικής ανοσίας εναντίον του παθογόνου παράγοντα. Τα σημαντικότερα είδη εμβολίων που παράγονται με βιοτεχνολογικές μεθόδους είναι τα εμβόλια-υπομονάδες, εμβόλια από ζωντανούς γενετικά τροποποιημένους ιούς και εμβόλια γυμνού DNA. Η παραγωγή των εμβολίων-υπομονάδων στηρίχθηκε στο γεγονός ότι όλα τα συστατικά ενός παθογόνου μικροοργανισμού δεν είναι απαραίτητα για την πρόκληση της ανοσολογικής αντίδρασης στον οργανισμό που θα προσβάλουν. Συνήθως, μόνο ορισμένες πρωτεΐνες επιφάνειας έχουν αντιγονική ιδιότητα. Τα εμβόλια-υπομονάδες στηρίζονται στην παραγωγή μόνο αυτών των συστατικών. Έτσι, γονίδια του παθογόνου μικροοργανισμού που κωδικοποιούν την πρωτεΐνη με την αντιγονική δράση εισάγονται σε κύτταρα που αναπτύσσονται σε κυτταροκαλλιέργειες και παράγουν την πρωτεΐνη αυτή σε μεγάλες ποσότητες. Στη συνέχεια, η πρωτεΐνη καθαρίζεται και χρησιμοποιείται ως εμβόλιο. Ένας άλλος τύπος εμβολίων είναι τα εμβόλια από ζωντανούς γενετικά τροποποιημένους ιούς. Στην περίπτωση αυτή γονίδια από επικίνδυνο ιό ή άλλο μικροοργανισμό ενσωματώνονται σε άλλο ιό, που είναι αβλαβής για τον άνθρωπο, όπως ο ιός της δαμαλίτιδας. Ο γενετικά τροποποιημένος ιός που προκύπτει εξακολουθεί να είναι αβλαβής, αλλά επειδή παράγει την αντιγονική πρωτεΐνη του ιού ή του μικροοργανισμού, εισάγεται στο σώμα και προκαλεί έντονη ανοσολογική αντίδραση (Εικόνα 8.3).
Εμβόλιο γυμνού DNAΈνας τύπος εμβολίου μπορεί να είναι το ίδιο το DNA. Στη συγκεκριμένη περίπτωση το γονίδιο που κωδικοποιεί την πρωτεΐνη με αντιγονική δράση εισάγεται κατευθείαν στον οργανισμό που πρόκειται να ανοσοποιηθεί. Το γονίδιο ενσωματώνεται στο γονιδίωμα και παράγει το αντιγόνο, το οποίο με τη σειρά του προκαλεί ενεργητική ανοσία στον οργανισμό. Η τεχνική εφαρμόστηκε πειραματικά σε ποντίκι. Η ενσωμάτωση είχε επιτυχία 75%. Ύστερα από τις απαραίτητες δοκιμασίες η τεχνική υπόσχεται πολλά για τον εμβολιασμό των οικόσιτων ζώων. |
ΑντιβιοτικάΤα αντιβιοτικά είναι χημικές ουσίες που παράγονται από μικροοργανισμούς και θανατώνουν άλλους μικροοργανισμούς ή αναστέλλουν την ανάπτυξη τους. Είναι προϊόντα του μεταβολισμού τους και σήμερα ορισμένα από αυτά παράγονται σε μεγάλες ποσότητες σε βιοαντιδραστήρες. Πολλά αντιβιοτικά μπορούν να συντεθούν και χημικά, αλλά η διαδικασία είναι τόσο ακριβή και επίπονη που δεν μπορεί να συγκριθεί σε κόστος με την παραγωγή από βακτήρια και από μύκητες. Η παγκόσμια χρήση των αντιβιοτικών για την καταπολέμηση των μικροβίων έχει βελτιώσει σημαντικά την υγεία των ανθρώπων και αναμφίβολα έχει σώσει εκατομμύρια ανθρώπινες ζωές. Έως σήμερα έχουν απομονωθεί από διάφορους μικροοργανισμούς, περισσότερα από 8.000 αντιβιοτικά με ποικίλους τρόπους δράσης. Η πλειονότητα των πιο σημαντικών αντιβιοτικών έχουν απομονωθεί από το βακτήριο του εδάφους, γένους Streptomyces, μολονότι και άλλα βακτήρια καθώς και μύκητες είναι πηγές αντιβιοτικών. Υπολογίζεται ότι αρκετές εκατοντάδες νέα αντιβιοτικά ανακαλύπτονται κάθε χρόνο ύστερα από εντατική έρευνα κατά την οποία ελέγχονται πολλές χιλιάδες διαφορετικοί μικροοργανισμοί, για να βρεθούν εκείνοι που παράγουν νέα αντιβιοτικά. Η τεχνολογία του ανασυνδυασμένου DNA άρχισε πρόσφατα να εφαρμόζεται με στόχο:
Γονιδιακή θεραπείαΠερισσότερες από 4.000 ασθένειες οφείλονται σε γονιδιακές μεταλλάξεις και πολλές από αυτές εμφανίζονται στις μεγάλες ηλικίες. Μερικές οφείλονται σε ένα μόνο γονίδιο, άλλες σε αλληλεπίδραση δύο ή περισσότερων γονιδίων και ακόμη περισσότερες σε συνδυασμό γενετικών και περιβαλλοντικών παραγόντων όπως η ακτινοβολία και οι χημικές ουσίες. Όλες σχεδόν οι γενετικές ασθένειες προκαλούν δυσμορφίες, το 80% όλων διανοητική καθυστέρηση και το ένα πέμπτο από αυτές θάνατο στην παιδική ηλικία. Έως πρόσφατα η μοριακή βάση των ασθενειών αυτών δεν ήταν γνωστή. Η τεχνολογία του ανασυνδυασμένου DNA σε συνδυασμό με τις μεθόδους της παραδοσιακής Γενετικής (γενεαλογικά δένδρα) οδήγησε στον εντοπισμό της θέσης στα χρωμοσώματα |
κεφάλαιο 8
(χαρτογράφηση) πολλών μεταλλαγμένων γονιδίων, που προκαλούν τις αντίστοιχες ασθένειες. Επιπλέον ορισμένα μεταλλαγμένα γονίδια κλωνοποιήθηκαν και συγκρίθηκαν με τα φυσιολογικά αλληλόμορφά τους, για να εξακριβωθεί το είδος των μεταλλάξεων. Η χαρτογράφηση όλων των γονιδίων στα χρωμοσώματα είναι ένας από τους κύριους στόχους του προγράμματος του ανθρώπινου γονιδιώματος, όπως θα αναφερθεί παρακάτω. Σήμερα έχουν χαρτογραφηθεί και κλωνοποιηθεί τα γονίδια των οποίων οι μεταλλάξεις είναι υπεύθυνες για ασθένειες όπως η κυστική ίνωση, η ασθένεια του Huntington και η μυϊκή δυστροφία Duchenne. Οι γνώσεις αυτές έδωσαν τη δυνατότητα ανάπτυξης θεραπείας που στηρίζεται στην τεχνολογία του ανασυνδυασμένου DNA και ονομάζεται γονιδιακή θεραπεία. Αυτή έχει ως στόχο να «διορθώσει» τη γενετική βλάβη εισάγοντας στους ασθενείς φυσιολογικά αλληλόμορφα του μεταλλαγμένου γονιδίου. Απαραίτητη προϋπόθεση για την εφαρμογή της γονιδιακής θεραπείας είναι, εκτός από την κλωνοποίηση του υπεύθυνου γονιδίου, και ο προσδιορισμός των κυττάρων που εμφανίζουν τη βλάβη από την ασθένεια. Η γονιδιακή θεραπεία εφαρμόστηκε για πρώτη φορά το Σεπτέμβριο του 1990 σε ένα τετράχρονο κορίτσι που έπασχε από ανεπάρκεια του ανοσοποιητικού συστήματος. Η ασθένεια αυτή οφείλεται στην έλλειψη του ενζύμου απαμινάση της αδενοσίνης (ADA), που παίρνει μέρος στον μεταβολισμό των πουρινών στα κύτταρα του μυελού των οστών. Η έλλειψη οφείλεται σε μετάλλαξη του γονιδίου που παράγει το ένζυμο αυτό. Η ασθένεια εμφανίζει αυτοσωμικό υπολειπόμενο τύπο κληρονομικότητας. Οι ασθενείς πάσχουν από χρόνιες μολύνσεις, έχουν προδιάθεση για ανάπτυξη καρκίνου σε πολύ μικρή ηλικία και πολλοί πεθαίνουν ύστερα από λίγους μήνες ζωής. Είναι γνωστή η περίπτωση ενός παιδιού που έζησε εννέα χρόνια σε έναν πλαστικό θάλαμο, για να εμποδιστεί η επαφή του με ιούς, επειδή το ανοσοποιητικό του σύστημα δεν μπορούσε να τους καταπολεμήσει. Η διαδικασία που ακολουθείται στη γονιδιακή θεραπεία της παραπάνω ασθένειας είναι η εξής:
Βέβαια τα τροποποιημένα λεμφοκύτταρα δε ζουν για πάντα μέσα στον οργανισμό -δηλαδή η θεραπεία δεν είναι μόνιμη- και χρειάζεται συνεχής έγχυση τέτοιων κυττάρων.
Εικόνα 8.4 Ex vivo γονιδιακή θεραπεία. |
Εικόνα 8.5 Γονιδιακή θεραπεία in vivo. Το φυσιολογικό γονίδιο μπορεί να εισέλθει στα κύτταρα του ιστού που εμφανίζει τη βλάβη, μέσω ιών, λιποσωμάτων και με τη μορφή «γυμνού DNA». Όμως, όπως στην περίπτωση των διαβητικών, τα άτομα μπορούν να ζουν φυσιολογικά, κάνοντας σε κανονικά χρονικά διαστήματα αυτή τη θεραπεία. Ο τύπος αυτός της γονιδιακής θεραπείας ονομάζεται ex vivo, γιατί τα κύτταρα τροποποιούνται έξω από τον οργανισμό και εισάγονται πάλι σ' αυτόν. Τα κύτταρα του αιμοποιητικού συστήματος μπορούν να τροποποιούνται γενετικά, να αναπτύσσονται σε κυτταροκαλλιέργειες και να εισάγονται με ενδοφλέβια ένεση στον οργανισμό. Τι γίνεται όμως αν πρέπει να τροποποιηθούν κύτταρα ενός άλλου οργάνου όπως ο πνεύμονας; Ο Anderson και οι συνεργάτες του πρότειναν μια άλλη προσέγγιση. Ανέπτυξαν «έξυπνους» φορείς, οι οποίοι προσβάλλουν τα κύτταρα του ιστού που πάσχει. Συγκεκριμένα, τα φυσιολογικά γονίδια ενσωματώνονται σε μόρια-φορείς, που εισάγονται κατευθείαν στον οργανισμό. Το είδος αυτό της γονιδιακής θεραπείας |
κεφάλαιο 8
ονομάζεται in vivo και εφαρμόστηκε για τη θεραπεία της κυστικής ίνωσης το 1993. Η κυστική ίνωση οφείλεται σε μεταλλάξεις ενός γονιδίου, το οποίο κωδικοποιεί μια πρωτεΐνη, που είναι απαραίτητη για τη σωστή λειτουργία των επιθηλιακών κυττάρων των πνευμόνων. Η ασθένεια παρουσιάζει υπολειπόμενη αυτοσωμική κληρονομικότητα και επηρεάζει πρωτίστως τη λειτουργία των πνευμόνων. Το φυσιολογικό γονίδιο ενσωματώθηκε αρχικά σε έναν αδενοϊό. Ο ανασυνδυασμένος ιός εισήλθε στον οργανισμό με ψεκασμό με τη βοήθεια βρογχοσκοπίου και μόλυνε τα κύτταρα του αναπνευστικού συστήματος. Μετά την εισαγωγή του στα κύτταρα, το φυσιολογικό γονίδιο ενσωματώθηκε στο γονιδίωμά τους και παρήγαγε το φυσιολογικό προϊόν (Εικόνα 8.5). Έως πρόσφατα η πιθανότητα επιτυχούς γονιδιακής θεραπείας ανήκε στη σφαίρα της επιστημονικής φαντασίας. Με τον προσδιορισμό γονιδίων που είναι υπεύθυνα για γενετικές ασθένειες και την εύρεση της αλληλουχίας τους δημιουργούνται νέες προοπτικές για τη γονιδιακή θεραπεία πολλών ασθενειών. Είναι βασικό να τονιστεί ότι παρόλο που η γονιδιακή θεραπεία παρουσιάζεται ως πανάκεια στην Ιατρική, η εφαρμογή της, τουλάχιστον στο άμεσο μέλλον, θα είναι περιορισμένη επειδή δεν έχουν ακόμη ξεπεραστεί προβλήματα όπως αυτά που αφορούν τη χρήση των φορέων. Όπως αναφέρθηκε προηγουμένως, στις περισσότερες περιπτώσεις ως φορείς χρησιμοποιούνται ιοί οι οποίοι αν και καθίστανται αβλαβείς, έχουν μικρή πιθανότητα να προκαλέσουν παρενέργειες και σε ορισμένες περιπτώσεις καρκίνο. Έτσι λοιπόν η ανάπτυξη πιο κατάλληλων φορέων είναι ο επόμενος στόχος για τη βελτίωση των μεθόδων της γονιδιακής θεραπείας, Με τις μεθόδους της γονιδιακής θεραπείας δε γίνεται αντικατάσταση του μεταλλαγμένου γονιδίου στα κύτταρα του οργανισμού αλλά ενσωμάτωση του φυσιολογικού αντιγράφου του στο γονιδίωμά συγκεκριμένων σωματικών κυττάρων. Συνεπώς δε μεταβιβάζεται στους απογόνους. Το πρόγραμμα ίου ανθρώπινου γονιδιώματοςΌπως έχει αναφερθεί, το ανθρώπινο γονιδίωμά αποτελείται από 3x109 ζεύγη βάσεων DNA, το οποίο κατανέμεται σε χρωμοσώματα. Η αποκρυπτογράφηση της αλληλουχίας βάσεων του DNA πιστεύεται ότι θα μας βοηθήσει να κατανοήσουμε πώς έχει «κατασκευαστεί» και λειτουργεί ο ανθρώπινος οργανισμός. Για το σκοπό αυτό το 1986 ξεκίνησε μια διεθνής συνεργασία με σκοπό τη χαρτογράφηση, δηλαδή τον εντοπισμό της θέσης των γονιδίων στα χρωμοσώματα, και τον προσδιορισμό της αλληλουχίας των βάσεων του DNA στο ανθρώπινο γονιδίωμά. Το πρόγραμμα, που φυσικά απαιτούσε τη συμβολή πολλών ερευνητών και γενναία χρηματοδότηση, ξεκίνησε το 1990 υπό την αιγίδα του Εθνικού Ινστιτούτου Υγείας και του Τμήματος Ατομικής Ενέργειας των ΗΠΑ Η Μοριακή Βιολογία με αριθμούςΑν η αλληλουχία των βάσεων του ανθρώπινου γονιδιώματος γραφτεί με κεφαλαία γράμματα χωρίς κενά, καλύπτει περίπου 1.000 βιβλία μεγέθους τηλεφωνικού καταλόγου. Κυστική ίνωση
Η κυστική ίνωση είναι μια εξαιρετικά σοβαρή ασθένεια, ιδιαίτερα διαδεδομένη ανάμεσα στους κατοίκους της Ευρώπης και των ΗΠΑ. Η θέση του γονιδίου που είναι υπεύθυνο για την ασθένεια αυτή βρίσκεται στο 7ο χρωμόσωμα και η δράση του σχετίζεται με τη δυνατότητα μεταφοράς ιόντων χλωρίου δια μέσου της κυτταρικής μεμβράνης. Χαρακτηριστικό σύμπτωμα της ασθένειας είναι η υπερβολική παραγωγή βλέννας στους πνεύμονες και στο γαστρενιερικό σωλήνα. Η συσσώρευση βλέννας παρεμποδίζει την αναπνοή και ο πάσχων παρουσιάζει έντονο βήχα. Η συσσώρευση βλέννας παρεμποδίζει επίσης την έκκριση του παγκρεατικού υγρού με αποτέλεσμα να μη γίνεται σωστά η πέψη των τροφών. Στη φωτογραφία η μητέρα χτυπάει στην πλάτη το παιδί του πάσχει από κυστική ίνωση για να βοηθήσει την απομάκρυνση της βλέννας από τους πνεύμονες. |
Αρχικά υπήρχε η εκτίμηση ότι το πρόγραμμα θα ολοκληρωνόταν το 2005, όμως, χάρη στην αυτοματοποίηση των εργαστηριακών μεθόδων και την ανάπτυξη της πληροφορικής, ολοκληρώθηκε το 2001. Η ανάλυση του ανθρώπινου γονιδιώματος θα συμβάλει:
Στην εικόνα 8.6 παρουσιάζονται οι εφαρμογές που προκύπτουν από την ανάλυση του ανθρώπινου γονιδιώματος.
Εικόνα 8.6 Εφαρμογές του προγράμματος του ανθρώπινου γονιδιώματος.
|
κεφάλαιο 8
Με την αποκρυπτογράφηση της αλληλουχίας του DNA θα γνωρίσουμε τον εαυτό μας.Πολλοί ερευνητές βρήκαν την προώθηση του προγράμματος του ανθρώπινου γονιδιώματος εξίσου ενδιαφέρουσα με την αποστολή του ανθρώπου στο φεγγάρι το 1960. Συνοψίζοντας το πρόγραμμα το 1989 ένας από τους συμμετέχοντες έγραφε ότι δεν είναι τίποτα περισσότερο από μία επιστημονική απάντηση στο ρητό του Σωκράτη «γνώθι σαυτόν». Οι προσπάθειες χαρτογράφησης ξεκίνησαν στις αρχές του 20ού αιώνα. Το 1913 συγκεκριμένα έκανε την εμφάνισή του ο πρώτος γενετικός χάρτης, που προσδιόριζε τη θέση των γονιδίων στο χρωμόσωμα Χ της μύγας των φρούτων (Drosophila melanogaster). Έως το 1950 οι γενετικοί χάρτες περιορίζονταν στην απεικόνιση της θέσης των γονιδίων μόνο στο Χ χρωμόσωμα διάφορων οργανισμών. Το 1968 εντοπίστηκε για πρώτη φορά η θέση γονιδίου σε αυτοσωμικό χρωμόσωμα. Το 1971 είχαν χαρτογραφηθεί στον άνθρωπο μόνο δεκαπέντε γονίδια, τα περισσότερα από τα οποία βρίσκονταν στο χρωμόσωμα Χ. Χάρη στο πρόγραμμα ανάλυσης του ανθρώπινου γονιδιώματος έως τα τέλη του 1998 είχαν χαρτογραφηθεί περίπου 13.000 γονίδια. 
Το πρόγραμμα αυτό χρειάζεται εκτός από τεράστια χρηματοδότηση, μια ισχυρή τεχνολογική υποστήριξη, η οποία βασίζεται:
Εδώ πρέπει να σταθεί κανείς στην ανεκτίμητη προσφορά της Βιοπληροφορικής και της ανάλυσης μέσω υπολογιστών. 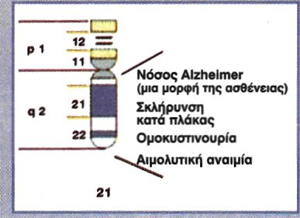
Ο όγκος των δεδομένων που παράγονται. δηλαδή τεράστιος αριθμός αλληλουχιών βάσεων DNA, θα ήταν αδύνατο να αναλυθεί και να συσχετιστεί χωρίς την ύπαρξη εξελιγμένων υπολογιστικών προγραμμάτων, καθώς και την αποθήκευσή τους σε βάσεις δεδομένων. Χαρτογράφηση γονιδίων που σχετίζονται με γενετικές ασθένειες στο χρωμόσωμα 21 και το χρωμόσωμα Χ. Έλεγχος φαρμακευτικών προϊόντων και μεθόδων θεραπείας ασθενειών.Όλα τα νέα προϊόντα και οι τεχνολογίες που εφαρμόζονται στον άνθρωπο περνούν από τέσσερις φάσεις ελέγχου, η καθεμία από τις οποίες διαρκεί δύο έτη. Οι φάσεις αυτές είναι οι εξής:
Συνολικά, ο έλεγχος διαρκεί περισσότερο από οκτώ χρόνια για να διαπιστωθεί αν αξίζει η εφαρμογή του φαρμάκου ή της μεθόδου σε ευρεία κλίμακα. Εισαγωγή γονιδίων στον άνθρωπο.Η επίσημη άδεια για εισαγωγή γενετικά τροποποιημένων κυττάρων στους ανθρώπους δόθηκε ύστερα από αρκετές διαδικασίες από το Εθνικό Ινστιτούτο Υγείας (ΝΙΗ) και τη Διεύθυνση Διατροφής και Φαρμάκων (FDA). Την απόφαση πήρε η Συμβουλευτική Επιτροπή του Ανασυνδυασμένου DNA (DNA advisory Comittee RAC) στις 3 Οκτωβρίου 1988 με ψήφους 16:5, κυρίως για λόγους συναισθηματικούς, «επειδή ένας άνθρωπος που πάσχει από καρκίνο δεν μπορεί να πάθει τίποτε χειρότερο». Ο ασθενής που επιλέχθηκε για να δεχτεί γενετικά τροποποιημένα κύτταρα ήταν 52 ετών και έπασχε από κακόηθες μελάνωμα, μια θανατηφόρο μορφή καρκίνου, που είχε κάνει μετάσταση στο ήπαρ. Η πρόγνωση ήταν δύο μήνες ζωής. Φυσικά δεν έγινε κανένα θαύμα, μολονότι ο ασθενής έζησε σχεδόν ένα χρόνο μετά την αρχική εμφύτευση των κυττάρων, το Μάιο του 1989, αρκετά περισσότερο χρόνο από ότι είχε προβλεφθεί. |
ΠερίληψηΗ τεχνολογία του ανασυνδυασμένου DNA βρίσκει ευρύτατη εφαρμογή στη μαζική παραγωγή φαρμακευτικών πρωτεϊνών, σημαντικότερες από τις οποίες είναι η ινσουλίνη, οι ιντερφερόνες, η αυξητική ορμόνη κ.ά. Η ανάπτυξη των ευαίσθητων τεχνικών παραγωγής και τροποποίησης των μονοκλωνικών αντισωμάτων δίνει τη δυνατότητα διάγνωσης ασθενειών πριν ακόμη εμφανιστούν τα συμπτώματα τους αλλά και τρόπους ανίχνευσης και θεραπείας διάφορων μορφών καρκίνου. Η βελτίωση της παραγωγής αντιβιοτικών και η παραγωγή νέων με μοναδικές ιδιότητες θα βοηθήσουν επίσης στη θεραπεία πολλών ασθενειών που οφείλονται σε παθογόνους παράγοντες. Η ανάπτυξη νέων, πιο εξειδικευμένων και χωρίς παρενέργειες εμβολίων υπόσχεται καλύτερη πρόληψη πολλών ασθενειών, για τις οποίες ήδη υπάρχουν εμβόλια. Η δημιουργία νέων εμβολίων εναντίον ασθενειών για τις οποίες δεν υπάρχουν εμβόλια, όπως το AIDS και ο καρκίνος αρχίζει να γίνεται εφικτή. Τέλος, η γονιδιακή θεραπεία βοηθά στην αντιμετώπιση γενετικών ασθενειών με εισαγωγή φυσιολογικού γονιδίου, στα σωματικά κύτταρα του οργανισμού που πάσχει από την ασθένεια. Το πρόγραμμα του ανθρώπινου γονιδιώματος είναι ένα τεράστιο ερευνητικό πρόγραμμα, που ξεκίνησε το 1986 και αποσκοπεί στην αποκρυπτογράφηση της αλληλουχίας του DNA και τον εντοπισμό της θέσης των γονιδίων πάνω στα χρωμοσώματα. Η ολοκλήρωση αυτού του προγράμματος θα συμβάλει στην κατανόηση του τρόπου λειτουργίας του DNA και θα έχει πολυάριθμες εφαρμογές στην Ιατρική και στη Βιοτεχνολογία.
Ερωτήσεις1. Ποια συστατικά χρειάζονται για να παραχθεί ανθρώπινη ινσουλίνη από κύτταρα Ε. coli;2. Σε ένα ευκαρυωτικό κύτταρο παράγεται ινσουλίνη:
3. Παρότι ο ποντικός και ο αρουραίος δεν είναι κτηνοτροφικής σημασίας ζώα, καταναλώνονται υπέρογκα ποσά για τη χαρτογράφηση του γονιδιώματός τους. Γιατί πιστεύετε ότι συμβαίνει κάτι τέτοιο;4. Αναφέρετε τα πλεονεκτήματα παραγωγής ανθρώπινης αυξητικής ορμόνης με μεθόδους Γενετικής Μηχανικής σε σχέση με την εξαγωγή της από πτώματα.5. Η ινσουλίνη ήταν η πρώτη πρωτεΐνη που παρήχθη με μεθόδους Γενετικής Μηχανικής. Για ποιο λόγο νομίζετε ότι παρήχθη η ορμόνη αυτή;6. Τι είναι τα εμβόλια-υπομονάδες;Εργασίες - ΔραστηριότητεςΠροετοιμάστε ένα μικρό λόγο διάρκειας τριών περίπου λεπτών που θα μπορούσε να παρουσιαστεί σε ραδιοφωνική εκπομπή με θέμα τη γονιδιακή θεραπεία. Αναφερθείτε στα επιμέρους προβλήματα και προοπτικές που δημιουργεί η τεχνική. |