 Εικ. 4.12 Ρούντολφ Κλαούζιους (1822-1888). Γερμανία. Ένας από τους θεμελιωτές της θερμοδυναμικής. Εικ. 4.12 Ρούντολφ Κλαούζιους (1822-1888). Γερμανία. Ένας από τους θεμελιωτές της θερμοδυναμικής.
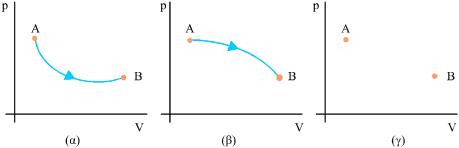
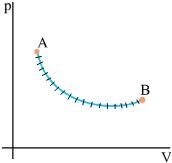 Σχ. 4.24 Σε μια αντιστρεπτή μεταβολή, η μεταβολή της εντροπίας υπολογίζεται αν χωρίσουμε τη μεταβολή σε πολύ μικρές μεταβολές και αθροίσουμε τις μεταβολές της εντροπίας σε κάθε απειροστή μεταβολή. Σχ. 4.24 Σε μια αντιστρεπτή μεταβολή, η μεταβολή της εντροπίας υπολογίζεται αν χωρίσουμε τη μεταβολή σε πολύ μικρές μεταβολές και αθροίσουμε τις μεταβολές της εντροπίας σε κάθε απειροστή μεταβολή. Σχ. 4.25 Στα διαγράμματα (α) και (β) ένα θερμοδυναμικό σύστημα μεταβαίνει από την κατάσταση Α στην κατάσταση Β με διαφορετικό κάθε φορά αντιστρεπτό τρόπο. Στο (γ) το ίδιο σύστημα μεταβαίνει από την κατάσταση Α στη Β με μη αντιστρεπτό τρόπο που δεν μπορεί να παρασταθεί γραφικά. Η μεταβολή της εντροπίας του συστήματος, είναι ίδια σε όλες τις περιπτώσεις. |
4-14 ΕΝΤΡΟΠΙΑ
Ο δεύτερος θερμοδυναμικός νόμος, όπως διατυπώθηκε στην προηγούμενη παράγραφο, δεν καταλήγει σε κάποια ποσοτική σχέση. Ποσοτική διατύπωση του 2ου θερμοδυναμικού νόμου έγινε δυνατή με την εισαγωγή μιας νέας έννοιας, της έννοιας εντροπία (σύμβολο S). Η εντροπία εισήχθη από τον Clausius, ο οποίος όρισε τη μεταβολή της εντροπίας (ΔS) συστήματος κατά τη διάρκεια μιας πολύ μικρής αντιστρεπτής μεταβολής, τόσο μικρής ώστε η θερμοκρασία του συστήματος να μπορεί να θεωρηθεί σταθερή, ως το πηλίκο του ποσού θερμότητας ΔQ που απορρόφησε ή απέβαλε το σύστημα προς τη θερμοκρασία του συστήματος.
Μονάδα της εντροπίας στο SI είναι το 1 J/K.
Όταν σε μια αντιστρεπτή μεταβολή το σύστημα απορροφά θερμότητα το ΔQ είναι θετικό, επομένως η εντροπία αυξάνεται. Όταν το σύστημα αποβάλλει θερμότητα το ΔQ είναι αρνητικό και επομένως η εντροπία μειώνεται.
Σε μια αντιστρεπτή μεταβολή κατά την οποία ένα θερμοδυναμικό σύστημα μεταβαίνει από μία αρχική κατάσταση Α σε μια τελική κατάσταση Β, η συνολική μεταβολή της εντροπίας μπορεί να υπολογιστεί αν χωρίσουμε τη διεργασία σε πολύ μικρές μεταβολές (Σχ. 4.24), υπολογίσουμε τη μεταβολή της εντροπίας σε κάθε μια από αυτές και αθροίσουμε όλους τους όρους.
Η μεταβολή της εντροπίας ενός συστήματος έχει την ίδια τιμή για όλες τις μεταβολές που οδηγούν από μία αρχική κατάσταση Α σε μία τελική κατάσταση Β, αντιστρεπτές ή μη.
Η μεταβολή της εντροπίας ενός συστήματος εξαρτάται μόνο από την αρχική και τελική του κατάσταση και όχι από το πώς πραγματοποιήθηκε η μεταβολή.
Ίσως βέβαια τα όσα είπαμε μέχρι τώρα να μη βοήθησαν καθόλου στο να κατανοήσετε την ανάγκη εισαγωγής αυτής της νέας έννοιας, της εντροπίας. |
Ελπίζουμε όμως στη συνέχεια να πεισθείτε για την χρησιμότητα του νέου μεγέθους.
Έστω ένα σύστημα που αποτελείται από δύο σώματα το Α και το Β, με θερμοκρασίες ΤΑ και ΤΒ αντίστοιχα. Το σύστημα είναι μονωμένο από το περιβάλλον (Σχ. 4.26). Αν ΤΑ>ΤΒ, θα μετακινηθεί θερμότητα από το σώμα Α στο Β. Το αντίστροφο το αποκλείει ο δεύτερος θερμοδυναμικός νόμος. Ας φανταστούμε μια αντιστρεπτή διαδικασία που μεταφέρει ένα πολύ μικρό ποσό θερμότητας ΔQ από το σώμα Α στο Β, τόσο μικρό ώστε να μπορούμε να λέμε ότι οι θερμοκρασίες των σωμάτων δεν μεταβλήθηκαν. Η μεταβολή της εντροπίας του σώματος Α θα είναι
Η εντροπία του συστήματος θα μεταβληθεί, κατά
Στο υποθετικό αυτό παράδειγμα, ο δεύτερος νόμος μάς οδήγησε στο συμπέρασμα ότι η εντροπία του απομονωμένου συστήματος αυξήθηκε. Το ίδιο συμβαίνει σε κάθε απομονωμένο σύστημα. Επομένως η έννοια της εντροπίας μάς επιτρέπει να επαναδιατυπώσουμε το δεύτερο νόμο ως εξής:
Κατά τη διάρκεια οποιασδήποτε μεταβολής ενός απομονωμένου συστήματος η εντροπία πάντοτε αυξάνεται.
Η εντροπία του συστήματος αποκτά τη μέγιστη τιμή της όταν επέλθει ισορροπία. Στην περίπτωσή μας το σύστημα ισορροπεί όταν εξισωθούν οι θερμοκρασίες των δύο σωμάτων.
Από ενεργειακή άποψη στο σύστημα αυτό αρχικά θα μπορούσε να λειτουργήσει μια θερμική μηχανή χρησιμοποιώντας σαν δεξαμενή ψηλής θερμοκρασίας το σώμα Α και σαν δεξαμενή χαμηλής θερμοκρασίας το σώμα Β. Η εξίσωση των θερμοκρασιών δεν παρέχει πια αυτή τη δυνατότητα.
Η αύξηση της εντροπίας ενός συστήματος οδηγεί στην ελάττωση της ικανότητας του συστήματος να παράγει ωφέλιμο έργο.
 |
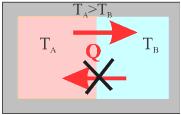 Σχ. 4.26 Η θερµότητα µεταφέρεται αυθόρµητα από σώµατα υψηλότερης θερµοκρασίας προς σώµατα χαµηλό-τερης. Το αντίστροφο αποκλείεται. Σχ. 4.26 Η θερµότητα µεταφέρεται αυθόρµητα από σώµατα υψηλότερης θερµοκρασίας προς σώµατα χαµηλό-τερης. Το αντίστροφο αποκλείεται.
Εικ. 4.13 Τα δύο χάλκινα ελάσματα όταν βρίσκονται σε διαφορετικές θερμοκρασίες αναπτύσσουν μεταξύ τους διαφορά δυναμικού που επιτρέπει τη λειτουργία του ανεμιστήρα. Στην περίπτωση (α) το σύστημα βρίσκεται σε ισορροπία, έχει τη μέγιστη δυνατή εντροπία και δεν έχει δυνατότητα παραγωγής έργου. Στην περίπτωση (β) το σύστημα δεν βρίσκεται σε ισορροπία, η εντροπία του είναι μικρότερη και έχει τη δυνατότητα παραγωγής έργου. |
Σχ. 4.27 (α) Σώμα πολύ χαμηλής θερμοκρασίας εκτελεί μεταφορική κίνηση. Όλα τα μόριά του έχουν την ίδια ταχύτητα (β) Το σώμα έχει συγκρουστεί με ακίνητο εμπόδιο. Οι ταχύτητες των μορίων έχουν τυχαίο προσανατολισμό. Η εντροπία, κατά τη σύγκρουση, αυξήθηκε. |
Μικροσκοπική ερμηνεία της εντροπίας
Στη δεκαετία του 1870 ο Boltzmann συνέδεσε την εντροπία, έννοια μακροσκοπική, με τη μικροσκοπική δομή του συστήματος και έδωσε στην έννοια νέο περιεχόμενο. Ο Boltzmann συνέδεσε το μέγεθος εντροπία με την αταξία που επικρατεί στα δομικά στοιχεία ενός συστήματος.
Όταν μεγαλώνει η αταξία που επικρατεί σε ένα σύστημα μεγαλώνει και η εντροπία του.
Έστω ένα σώμα πολύ χαμηλής θερμοκρασίας (κοντά στο απόλυτο μηδέν), που κινείται με ταχύτητα υ. Τα σωματίδια από τα οποία αποτελείται το σώμα έχουν όλα τη μεταφορική ταχύτητα υ του σώματος και λόγω της πολύ χαμηλής θερμοκρασίας είναι σχεδόν ακίνητα ως προς αυτό. Η κινητική ενέργεια του σώματος είναι, σχεδόν, όση και το άθροισμα των κινητικών ενεργειών των μορίων του. Το σώμα στην πορεία του συναντά ένα εμπόδιο και συγκρούεται. Κατά τη σύγκρουση δε χάνεται ενέργεια. Αν αθροίσουμε τις κινητικές ενέργειες των μορίων του σώματος μετά τη σύγκρουση η ενέργεια που θα πάρουμε είναι όση και πριν. Για να είμαστε πιο ακριβείς, στους υπολογισμούς μας θα πρέπει να συμπεριλάβουμε και την αύξηση των κινητικών ενεργειών των μορίων του εμποδίου γύρω από το σημείο της σύγκρουσης.
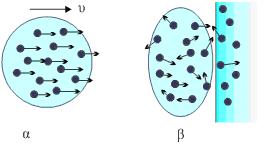
Όμως, ενώ πριν συγκρουστεί τα μόρια του σώματος είχαν όλα την ίδια ταχύτητα (Σχ. 4.27α) μετά τη σύγκρουση τα μόρια κινούνται άτακτα προς όλες τις κατευθύνσεις (Σχ. 4.27β). Πριν τη σύγκρουση το σώμα είχε κάποια κινητική ενέργεια η οποία θα μπορούσε να χρησιμοποιηθεί για την παραγωγή έργου, λόγου χάριν θα μπορούσε να καρφώσει μια πινέζα στον τοίχο. Μετά τη σύγκρουση η συνολική ενέργεια δεν άλλαξε είναι όμως αδύνατον πια να εκμεταλλευτούμε την ενέργεια του συστήματος. Η αταξία του συστήματος αυξήθηκε, μετά τη σύγκρουση. Αν μπορούσαμε να τη μετρήσουμε θα διαπιστώναμε ότι η εντροπία αυξήθηκε.
Από μακροσκοπική άποψη η αύξηση της εντροπίας οδηγεί σε μείωση της ικανότητας για παραγωγή έργου, ενώ από μικροσκοπική άποψη η αύξηση της εντροπίας οδηγεί σε αύξηση της αταξίας του συστήματος. |
|
Εικ. 4.14 Τα Γλαρονήσια, στα βόρεια της Μήλου, έχουν προκύψει από ηφαιστειακή δράση. Η λάβα κατά την ψύξη της πήρε ασυνήθιστα γεωμετρικά, ραβδόμορφα σχήματα. Η εντροπία της λάβας μειώθηκε. Δεν γνωρίζουμε κάτω από ποιες συνθήκες συνέβη αυτό. Εκείνο για το οποίο μπορούμε να είμαστε βέβαιοι είναι το ότι καθώς μειωνόταν η εντροπία της λάβας, αυξανόταν η εντροπία του περιβάλλοντος.
|