Η συμπλήρωση των οργανικών αντιδράσεων οξείδωσης - αναγωγής, όπως αυτών που αναφέραμε παραπάνω, γίνεται με την ίδια σκέψη που κάναμε για τη συμπλήρωση την των ανόργανων αντιδράσεων οξειδοαναγωγής.
Η συνολική μεταβολή του Α.Ο. σε μια οργανική ένωση την μπορεί να υπολογιστεί με βάση τους εξής πρακτικούς κανόνες:
α. Όταν μια οργανική ένωση χάνει 1 άτομο Η ή 1 άτομο αλκαλίου (π.χ. Na ή Κ) έχουμε αύξηση Α.Ο. = 1. Στην πραγματικότητα οξειδώνεται κάποιο άτομο C, αλλά αυτό δε μας απασχολεί για τη συμπλήρωση των αντιδράσεων.
β. Όταν μια οργανική ένωση κερδίζει 1 άτομο οξυγόνου, έχουμε αύξηση Α.Ο. = 2.
Παράδειγμα 7.7
α. Οξείδωση RCH2OH σε RCOOH με διάλυμα KMnO4 παρουσία H2SO4
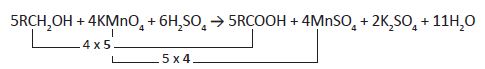
Κατά την οξείδωση αλκοόλης RCH 2OH σε καρβολικό οξύ RCOOH παρατηρείται αύξηση. Α.Ο. = 4, γιατί η αλκοόλη χάνει 2 άτομα Η και κερδίζει 1 άτομο οξυγόνου (2+2=4).
β. Οξείδωση RCH2OH σε RCOOH με διάλυμα K2Cr2O7 παρουσία H2SO4.
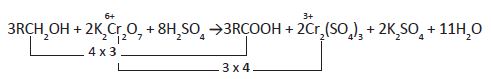
Κατά την οξείδωση RCH 2OH → RCOOH η συνολική αύξηση του Α.Ο., όπως αναφέρθηκε στο προηγούενο παράδειγμα, είναι 4.
γ. Οξείδωση HCOOH σε CO2 με διάλυμα KΜnO4 παρουσία H2SO4.
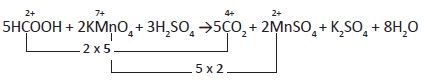
Εδώ η μεταβολή του Α.Ο. του C από το HCOOH στο CΟ 2 είναι 2.
δ. Η οξείδωση (COONa)2 σε CO2 με KMnO4 παρουσία H2SO4
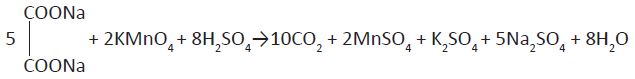
H συνολική αύξηση Α.Ο. του (COONa) 2 είναι 2, καθώς το άλας χάνει κατά την αντίδραση 2 άτομα Na.
|